

Для начала, мы скажем, что мы делаем полиуретаны из двух мономеров, двухосновного спирта и диизоцианата. Можно ли нам взглянуть на них? Да, конечно, вот они как раз на рисунке ниже:
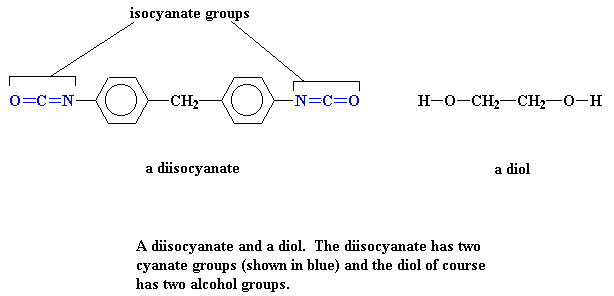
Вы можете увидеть также и их трехмерные модели, нажав сюда, если захотите.
При помощи вот этой маленькой молекулы под названием диазодицикло(2,2,2)октан (diazobicyclo[2.2.2]octane), или сокращенно DABCO, мы можем заставить эти два мономера полимеризоваться. Когда мы смешиваем эти два мономера с DABCO, происходит нечто любопытное.
DABCO является очень хорошим нуклеофильным реагентом или электроно-донорным веществом. Это означает, что у него есть пара неподеленных электронов, которая с превеликим удовольствием присоединится к какому-нибудь легко уязвимому ядру. Как вы помните, у электронов заряд отрицательный, а ядра атомов несут на себе положительный заряд. И все мы знаем, что отрицательные и положительные заряды притягивают друг друга. Поэтому электроны в молекуле будут смотреть по сторонам и обнаружат ядро у одного из атомов водорода в гидроксильной группе двухосновного спирта. Эти атомы водорода уязвимы, поскольку они соединены с атомами кислорода. Кислород обладает высокой электроотрицательностью. Это означает, что он притягивает к себе электроны от соседствующего с ним атома водорода. Это нарушает равновесие в атоме водорода между положительным зарядом ядра и отрицательным зарядом электронов. Электроны могли бы уравновесить положительный заряд ядра своими отрицательными зарядами, не будь они так сильно притянуты к кислороду. Это оставляет атом водорода с небольшим положительным зарядом.
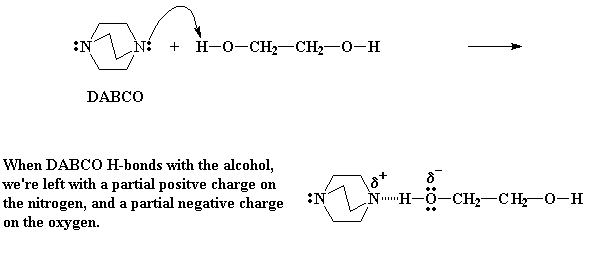
Так что электроны в молекуле DABCO видят это и просто не могут удержаться. Они бросаются вперед и образовывают водородную связь между атомом водорода одной из гидроксильных групп в молекуле двухосновного спирта и атомом азота в молекуле DABCO. Эта водородная связь оставляет частичный положительный заряд на атоме азота, но еще важнее то, что в результате образуется частичный отрицательный заряд на атоме кислорода. Этот частичный отрицательный заряд просто выводит атом кислорода из себя. И поскольку он вышел из себя, ему хочется с чем-нибудь провзаимодействовать.
Хотите ли вы узнать, с чем же именно он прореагирует?
У атома кислорода электроны в избытке, поэтому он и провзаимодействует с чем-нибудь, у чего недостаток электронов. Если мы посмотрим на нашу молекулу диизоцианата, то мы увидим, что атом углерода в изоцианатной группе зажат между двумя электроотрицательными атомами, кислородом и азотом. Это означает, что этот атом углерода испытывает действительно острую необходимость в электронах. Поэтому наш горячий атом кислорода времени не теряет и взаимодействует с ним. Он дает пару электронов атому углерода и образуется связь.

Конечно же, это выталкивает пару электронов из двойной связи между атомами азота и кислорода. Эта пара теперь обосновывается на атоме азота, сообщая ему отрицательный заряд. Тем временем наш атом кислорода, подарив пару электронов, остается с положительным зарядом.
Нет ничего на свете, что атом азота любил бы меньше, чем иметь отрицательный заряд. Поэтому он стремится от него избавиться, как только представится для этого возможность. Самым простым способом является подарить эту пару элетронов нашему старому знакомому, атому водорода в спиртовой группе. В результате образуется связь между атомами водорода и азота.
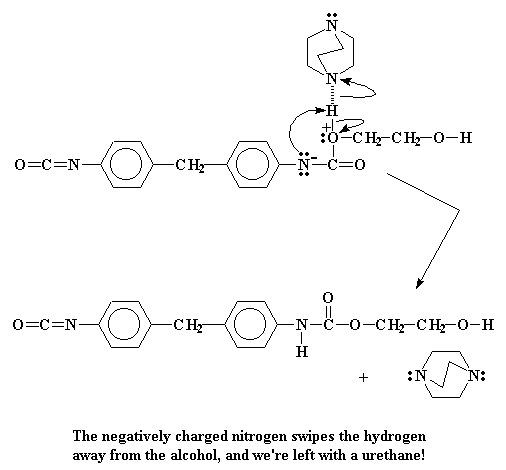
Электроны, которые этот атом водорода раньше делил с атомом кислорода, теперь безраздельно принадлежат самому кислороду. Это устраняет старый положительный заряд, который нес на себе атом кислорода. Когда все закончится, у нас остается новенький с иголочки уретановый димер.
У этого уретанового димера на одном конце молекулы находится спиртовая группа, а на другом - изоцианатная группа. Поэтому он может провзаимодействовать либо с двухосновным спиртом, либо с диизоцианатом, образовав тример. Или он может прореагировать с другим димером, тримером или даже более крупным олигомером. Таким образом, мономеры и олигомеры продолжают взаимодействовать и соединяться до тех пор, пока мы не получим полиуретан с высокой молекулярной массой.
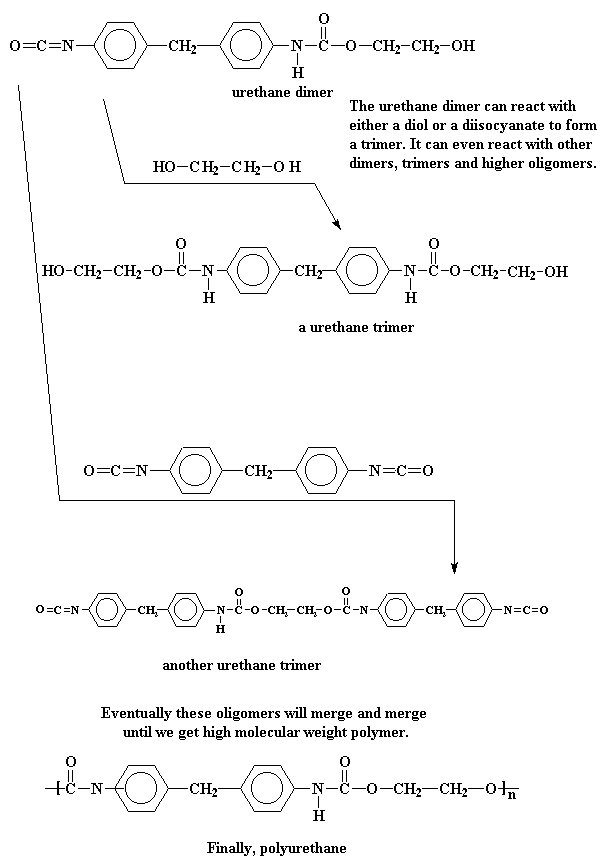
Те из вас, кто ведет дома записи наших занятий, могут заметить, что при образовании полиуретана могут взаимодействовать не только мономеры, но также и димеры, тримеры и так далее. Поэтому эту реакцию можно отнести к типу ступенчатой полимеризации. А поскольку при этом не образуется низкомолекулярных побочных продуктов, эта реакция также является полимеризацией присоединения.
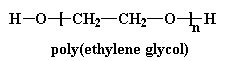
В результате мы получаем, так сказать, полимер внутри полимера, а образующийся полиуретан выглядит примерно вот так:
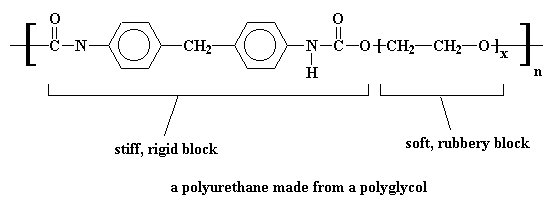
Вы можете, если захотите, также узнать, как делается вспененный полиуретан.
 Вернуться на страницу Полиуретаны
Вернуться на страницу Полиуретаны
 Вернуться в директорию Четвертого Уровня
Вернуться в директорию Четвертого Уровня Вернуться в основную директорию Макрогалереи
Вернуться в основную директорию Макрогалереи